「研究技術」を求める・持つうえでの理念・考え方(2014. 6月 宮田 記)
当研究室では,「脳がどのようにできてくるか」を深く知るためには「細胞のふるまい」を理解することが きわめて重要である と考えています.たとえば,ある分子「X」が失われて脳形成に重大な事態が生じたとき「分子 X は 脳形成にとって,『とても重要である』『不可欠である』」と言えますが,もし「細胞たちがどう暮らしているか」を知らないままでは,「どう重要」なのか,すなわち「細胞たちによって『どう 分子 X が使われている』のか」を具体的に言うことが難しいからです.
このように,私たちは,「脳の作られ方」を深く理解するということは,ひとつには「細胞の生き様を充分に知った上で細胞内外の分子機構を読み解く」ということであると考えています.この「細胞→分子」という「分解」の方向の理解の「足場・立脚点」として「細胞たちのふるまい」の理解が必要であるという「心構え」に加えて,私たちは,さらに「単一細胞→細胞群→組織」という「集合・階層上昇」の方向の軸上で「細胞のふるまい」の「意味」を問うていくということも重要であるとの意識,すなわち「『全体』への志向性」も持っています.
こうした願いのもと,「細胞たちのふるまい」と「それを担うしくみ」および,いろいろなふるまいを示す細胞たちの「集い方・群れ方」についての探求に役立つさまざまな方法論,技術に関心を持ち,新しい手法を取り込みあるいは開発しながら研究を行なっています.関西にも関東にも岡崎市(自然科学研究機構)にも近いという名古屋の「地の利」を活かしての「腰の軽い」交流・修行旅を大切と考えています.動物としては,おもにマウスを用いています.以下に,現在よく実施している解析の仕方を紹介します.
技術・手法
1.組織学的手法
特定のタンパク質の発現パターンの調査や実験(遺伝子操作や薬剤による)の結果判定(細胞増殖,分化,移動についての)などの目的で行ないます,脳原基や胎仔あるいは培養に供した組織塊などに対して,「パラホルムアルデヒド」を含有する液による「固定」(胎生13日目以降の胎仔は実体顕微鏡下の経心的な灌流による)を施し,凍結切片作成ののち,免疫組織化学検査を施し,蛍光顕微鏡による観察・記録,撮影したデジタル画像の解析へと進みます.
組織像の「読み解き」には,①これまでの豊富な組織染色の経験,②「『培養』で得た,生きた細胞たちのかたちとふるまいについての情報」(後述),③単一細胞遺伝子発現による細胞プロファイリングの情報(後述)が役に立ちますので,当研究室を訪れた学生さんは,「正常・異常の診断力」を磨くことができます.また,最近,深澤有吾博士(福井大学)のご協力のもとSerial block face 走査電顕(SBF SEM)によって,ライブ観察で見いだした特殊構造体の生体内での実在の証明を行なうなども実施中です.通常の走査電子顕微鏡ならびに透過型電子顕微鏡については,名古屋大学医学系研究科の共通機器利用を通じて実施可能です(一例:2013 Figure S2).
2.細胞・組織の培養とライブ観察
「スライス培養」は,当研究室を特徴づける手法です.宮田は90年代前半に小川正晴先生から,Sally Temple(1989) 風の「単離した神経幹細胞の低密度培養法」(1平方センチあたり1000細胞かそれ以下なので,分裂の様子が位相差顕微鏡で把握できる)を教わった一方で,プラスティック皿上で「組織塊」が「細胞シート」へと広がる培養(1994)や,小脳原基をコラーゲンゲルへ埋めてプルキンエ細胞の配置を再現する培養(1997)をやってみるなど3次元性への志向性を持ち,やがて「本来の組織中での形態をとらせたままで単一神経幹細胞の分裂」を捉えるスライス培養の報告に至りました(2001).
スライス中の個々の細胞の形態描写は,散発的な蛍光標識によってなされます.当初用いていたのは,脂溶性蛍光色素DiI の微細粒子(直径10 um以下)であり,「脳原基の脳膜面あるいは脳室面から低濃度で与えた粒子がきわめて散発的にランダムに付着したごく一部の細胞の全身」を染めるという方法でした(2001, 2003,2004, 2007, 2009など)が,最近は,子宮内エレクトロポレーション法(Fukuchi-Shimogori et al; 2001; Saito & Nakatsuji 2001; Tabata & Nakajima 2001)によって「蛍光蛋白(GFPなど)発現ベクターとcreリコンビネースを発現させるベクターを混合して導入する手法(Morin et al., 2007)」を頻用します(2009〜).遺伝子ノックダウンと蛍光標識を組み合わせること可能です(2013).また,細胞内のオルガネラやタンパク質の動態を観察することもできます(2013),ちなみに「DiI 法」には,胎仔・脳原基の採取から2時間程度で観察が始められるという即座性に加えて,細胞形態に依存しての標識がなされるという特長があります(脳膜側すなわちbasal側からの標識で,「脳膜面まで伸びた前駆細胞(幹細胞的)」に加えて,すでに移動を終えたニューロンを散発的に可視化できます: 2001.いっぽう脳室側すなわちapical側からの標識では「待ち針型(pin-like)細胞」を効率的に,経験則的にはほぼ「狙う」に近い感じで,可視化することができます:2007, 2009).
当研究室では,主にマニュアルで(「徒手的」に)スライスを(微小メス [眼科の角膜手術に用いられるような] を用いて,培養液をたたえたシリコンラバー「まな板」上で)作成します(自動スライス機を使うことは稀です).徒手法では,観察に適する断面上の細胞配向を考えてスライスすることができます.また,組織内残留応力解法試験(後述,2013 Figure 4, 6)や,特定の層(ニューロンの層や前駆細胞の層)の切り分け(「外科的細胞ソーティング」2013 Fugure 8g,h )にも微小メス操作が役立ちます.
作成されたスライス(厚さ 0.2-0.3 mm)は,プラスティック皿中でコラーゲンゲルによって不動化され,人力による(インキュベーターと顕微鏡ステージの間を往復する)あるいは自動的な制御による経時観察・撮影に供されます(ゲルは最終濃度 0.8 mg/ml 程度で用いますが,スライスの成長を充分に許容する程度に柔軟で,視野揺動を防ぐ程度の強度を有します).
培養液は,幹細胞の分裂を支えるような汎用的なものです.40%酸素を与えることで,スライス深部での虚血によるダメージを補なおうとしています(2002).スライス中の細胞の生存は長く続きますが,本来の三次元状況の維持を重視して,ライブ観察は多くの場合2日間までとしています.スライスを作成した後に薬剤実験を行なうこともできます(2006, 2007, 2009).「スライス中でライブ観察した細胞」がどんな分子を発現しているか,観察後に固定して免疫染色することもできます(この手技は「ライブで見た細胞」を,固定操作や切片作成のための手づつきの間に「見失う」ために意外に難しく,他研究室での実施例はきわめて少ないですが,当研究室は得意にしています: 2001, 2004, 2007, 2009, 2014).
最近,従来行なってきた「スライス中の単一細胞の観察」に加えて,「スライス中の全細胞の観察」も行なうようになりました(2013〜).供与された「すべての細胞の細胞膜(lyn-Venus により)あるいは核(H2B-mCherry により)が光るようなトランスジェニックマウス」(2011, 藤森俊彦博士 [基礎生物学研究所])からスライスを作成,または,細胞膜に対して親和性のある蛍光色素(bodipy ceramide や FM-4-64)による標識を行なってからスライスし,スピニングディスク型の共焦点顕微鏡による観察を行ないます.また,「分化傾向にある細胞すべて」の可視化のために独自にトランスジェニックマウス(Neurog2-d4Venus line および Gadd45g-d4Venus line)を作成しました(2014).
これまで,マウス大脳皮質原基をメインの研究対象とし,胎生中期(E12-15)でのスライス培養を行なってきましたが,他に,胎生期マウス小脳(2010, 2014),胎生期マウス網膜(2003, 2014),胎生期マウス脊髄(2014),胎生期フェレット大脳皮質(2014),ニワトリ胚の各所など,幅広く「スライス培養」を行なうことができます.正常マウス由来の脳原基部域とミュータントマウス由来の部域を「共培養」してスライス内の細胞移動を観察する(2002)などの応用も可能です.
当研究室を訪れた学生さんは,このようなさまざまな「細胞への向き合い方」の歴史・変遷を学びつつ,目的に応じたあの手この手の工夫を自ら主体的に思案し,あみ出していくことができるよう,基本的には見守りに似た,「緩やかな指導」を受けることになります.
3.遺伝子発現についての解析と遺伝子操作実験
「見る」ということで「個」と「全体」をつなごうとする当研究室は,一方で,遺伝子レベルの解析でも「個」の理解に根ざす「全体の俯瞰」を目指しています.脳原基の中で神経前駆細胞が集まっている箇所は,以前は「均一」であると見なすしかありませんでした.研究史上早い年代に「前駆細胞マーカー」として見いだされた分子(例えばネスチンなど)に対する免疫組織化学でどの細胞もが同様に染まる,というのがその「均一視」の拠り所でした.しかし「2」で紹介したようなライブ観察の手法で,細胞のふるまいをじかに見てみると,同じ場所に居てもちがう仕事をする神経前駆細胞が確かに存在する,と分かってきました.具体的には,未分化な「幹細胞」的な前駆細胞とは別に,分化傾向にある(細胞産生ポテンシャルとしては,「幹細胞」が最大なのに対して,低い,すなわち「ニューロンづくり専門」である)前駆細胞(lineage-restricted progenitor)が混じっていると分かってきたのです(2004).そうした情勢を踏まえて,理研CDBの松崎文雄博士のグループでは,前駆細胞の大集団のなかに実在する多様性を遺伝子発現に注目して理解し,その多様性の維持や変容の原理をやはり遺伝子発現パターンから読み解き,そうした努力を通じて「全体」のありようを説明しよう,という研究を始めました.単一細胞の遺伝子発現を網羅的にマイクロアレイを用いて解析し,細胞プロファイリングすることを通じて,同じステージでの多様性,発生ステージ依存的な変化などを理解するという取り組みです.同グループでその研究(2008)を推進した川口(現在,当研究室の准教授)が,このアプローチを用いてのさらなる研究を進めています.
それにあたり「子宮内エレクトロポレーション法」(前述:ライブ観察目的の蛍光標識の箇所で)による遺伝子強制発現あるいはノックダウン実験が日々行なわれています.「時に応じた前駆細胞の『気持ち』の変化」を読み解くには,我々に「タイムマシン的実験」(特定の遺伝子が時期特異的に発現する場合,時期を変えて強制発現------heterichronic expression-----させてみる)を行なう能力があることが役立ちます.当研究室では,胎生期のいろいろなタイミングで遺伝子導入を行なう技術を持っています(一般的によく行なわれる胎生中期におけるエレクトロポレーションに加えて,胎生10日目マウスの大脳原基への遺伝子導入が行なわれています).「胎生10日目」への「子宮内エレクトロポレーション法」は技術的にかなり難しいのですが,当研究室では理研 BSI の下郡智美博士(開発者 2001)から教わり,ほぼ日常的に実施しています(2013).学生は, in situ hybridization や PCRによる解析などを含めた基本的技術に加えて,「現場意識」のもと目的に応じてきめ細やかに行なわれている一連の解析法を習得することができます.
4.画像データ解析,定量的解析
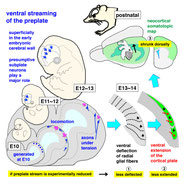
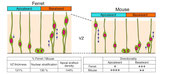
ライブ観察の対象が「組織中の単一細胞」から「全細胞」へと膨らむにあたり,集団内の「動き」の多様性を念頭に,定量的な解析を行なうようになりました.平均二乗変位(mean square displacement, MSD)法は,ある対象の動きかたが,directional(「一途」いちず)か 否(逡巡的, fructuating, random)かを客観的に教えてくれる解析法です.当研究室では,このMSD法を上田昌宏博士(大阪大学)から教わり神経前駆細胞および娘細胞の核の動き方(interkinetic nuclear migration, INM)の解析に用いました.そして,① 誕生時に「basalファイバー」を親細胞から相続した娘細胞と「非相続」の娘細胞とでは誕生地であるapical面からのbasal方向への(basalward)核の初動に差がある(細胞物流上のボトルネックへの対処として basal ファイバー依存的な「時差出勤」機構がある,2013 [下図] ),② マウスとフェレットでは INM の様態に大きな違いがある(マウスでは directionality が,apicalward > basalward であるのに対して,フェレットでは apicalward < basalward である)(2014)との発見につながりました.なお,核の軌跡の把握・解析は市販のソフトを用いていますが,核の追跡のための「対象指定」は,自動ではなく人力で(動画をモニターで見ながら研究者めいめいが)行なっています.この他にも,「集団のありよう」の理解に役立つ解析法をさまざまな系(上皮やその他の細胞システム)にならって行なえるよう情報の収集,専門家との交流に務めています.

5.力学的手法
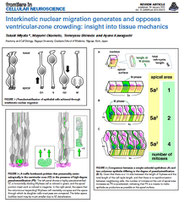
生体内で組織中にはいろいろな力がかかっていると予想されます.スライス中で「全細胞の観察」をしてみると,隣近所同士で押し合いへしあいしていることがうかがえます(たとえば,分裂中の細胞が膨らむ時,すぐ隣りの細胞の細長いファイバー状のからだがグニャリと曲げられるのが見えたりします).正常な状態でそのような細胞密度,「生理的混雑」にある細胞たちは,いったん集団としての移動に支障をきたし大渋滞に陥ると,過剰な力学的負荷にさらされます.「過剰」であると分かる,その判断の根拠となるのが,「組織内残留応力解放試験」の結果です.例えば,生体内(胎仔の頭のなか)で「半球」構造をしている大脳皮質原基の壁は,とりだしてスライスすると,30分以内に「apical側に曲がる・巻く」という変化を示します(2013, 下図 B).これは,apical面(神経前駆細胞と娘細胞たちのエンドフットがアドヘレンスジャンクションで寄せ合わされるて構成される)の収縮性(アクトミオシン依存的な)によると考えられます(apical面の収縮性はいろいろな上皮に共通です).apical面の収縮性は,面を直視して,メッシュに対して微小レーザー照射を施す(焼灼する)と,焼灼点から遠心的にメッシュ断端が広がるように動くという結果からも分かります(2013, 下図 A.理研CDBの林茂生博士・近藤武史博士にご協力いただきました).TAG-1を奪う実験によって「背低」になり大渋滞を起こした細胞たちは,壁のこわばり(図B),メッシュの「目」のしつこい広がり(図A)を示しました.apical面のすぐそばでの「かさばり(核および細胞体の渋滞)」のせいで,apical面の収縮性が充分に発揮できず「曲がり・巻き」が鈍ったという訳です.
こうした「応力解放試験」に加えて,当研究室では原子間力顕微鏡(atomic force microscope, AFM)を用いて,組織の「硬さ」(弾性率)を測定するということも始めています.細胞が置かれた三次元環境の物理的要因が細胞の挙動にどんな影響を及ぼすか,既定の方法論はないので,細胞社会の現場の事情を踏まえて柔軟かつ大胆に新しい実験系を構築することになります.

6.シミュレーション
「全細胞のイメージング」を行なうようになり,私たちは,すべての細胞の動きを見ながら,「個別の動きが とにかく うまく寄せ集まって,いつ見ても全体としてきれいな組織構造がとれている」ことを体感するようになりました.「ある細胞の核が apicalward に動く時に 隣りの・別の細胞はそれとは違う動きをしており,非同調的な,おそらくは一定の多様さを内在するであろうような『動きたち』がどうにか組み合わさって,全体として 変な殺到 や 渋滞・よどみがない ということになっている」のを,ひとまず「見る」ことができるようになりました.
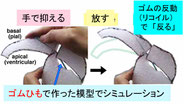
この「うまいありよう」自体は,じつは,私たちが意識しないままに「組織学」によってすでに分かっていました(いつ固定して切片を作成しても整然と細胞が詰め込まれていると,昔から分かっていました).しかし,「ありよう」を生で直視し始めたのはまさに今であり,すると,この「今やっとできるようになったすべてを見る」ことが,「どう皆で『うまくやっている』のか」という「今ならでは」の新しい問いを提示していると思えます.この「集団が集団として動くことを可能にしているルール(がもしあるならばぜひそれ)」を明らかにしたいという願いを叶えるために,私たちはコンピューターシミュレーションを用いることにしました.「見た」情報を忠実に反映して「真似てみる」ことを通じて「原理・ルール」のようなものを見いだすことができるのではないかと考えたからです.私たちはライブ観察情報をふんだんに持っていますので,それを,シミュレーションの「お手本」として用いることができます.専門家(三浦岳博士 [九州大]・長山雅晴博士 [北海道大])に interkinetic nuclear migration の数理モデルを作っていただき「現場」(私たちの感覚)とすり合わせるという流れで研究を進めています.
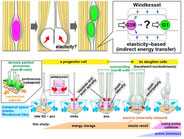
組織内の力学的な状況の理解のためにもシミュレーションが有用です.上記の「TAG-1 欠損による神経前駆細胞の過剰混雑」を模すシミュレーション(安達泰治博士・井上康博博士 [京都大学]による)が,「凹になったapical面付近での過剰混雑は,組織ユニットのbasal方向への離脱へとつながる」との結果をもたらしました(Okamoto et al., 2013).これを受けて,当研究室では,上記の「AFMによる実測」や「応力解放試験」の結果も参考にしながら,細胞形態を反映した新しい力学モデルを得られるように取り組もうとしています.
リソース
トランスジェニックマウス
1. Neurogenin2 (Neurog2)-d4Venus mouse
Acc. No.
CDB0490T: http://www.cdb.riken.jp/arg/TG%20mutant%20mice%20list.html
2. Gadd45g-d4Venus mouse
Acc.
No. CDB0491T: http://www.cdb.riken.jp/arg/TG%20mutant%20mice%20list.html
いずれも Kawaue et al. 2014 に詳しく紹介しています.脳,脊髄の原基,網膜など,神経系のあちこちで(Neurog2-Tg Gadd45g-Tg それぞれに部位特異性あり)「分化傾向にある」細胞が光ります(分化し切ったニューロンではなく「分化途上」の細胞を対象として,網羅的識別,形態観察などが可能です).